Внутренняя геометрия кристаллов, глава из Физики сплошных сред
Все статьи этой группы рассчитанны на аудиторию, имеющую базовую подготовку. Материалы рассчитаны на лиц, имеющих полное среднее образование, студентов и лиц, имеющих высшее образование научно-технического профиля. Лицам, имеющим гуманитарное и неоконченное среднее образование, материалы могут представлять значительные трудности для чтения и освоения и будут непонятны. Изложена глава 1 из книги Р.Фейнмана, Р.Лейтона, М.Сэндса "Фейнмановские лекции по физике", том 7 "Физика сплошных сред".
- Как растут кристаллы, математическая модель физического процесса new!!
- Внутренняя геометрия кристаллов, глава из Физики сплошных сред
- Рост кристаллов и кристаллические решетки, симметрия кристаллов
- Дислокация и рост кристаллов, физические модели роста кристаллов
§ 1. Внутренняя геометрия кристаллов
Начнем с изучения твердых тел, точнее кристаллов. Если атомы в веществе движутся не слишком активно, они сцепляются и располагаются в конфигурации с наименьшей возможной энергией (по сути дела, задача на минимакс из методов оптимизации: стремление минимизировать свою максимальную энергию). Если атомы где-то разместились так, что их расположения отвечают самой низкой энергии, то в другом месте атомы создадут такое же расположение. Поэтому в твердом веществе расположение атомов повторяется.
Иными словами, условия в кристалле таковы, что каждый атом окружен определенно расположенными другими атомами, и если посмотреть на атом такого же сорта в другом месте, где-нибудь подальше, то обнаружится, что окружение его и в новом месте точно такое же. Если вы выберете атом еще дальше, то еще раз найдете точно такие же условия. Порядок повторяется снова и снова и, конечно, во всех трех измерениях. Речь идет о периодически повторяющемся элементе.
 Представьте, что вам нужно создать рисунок на обоях или ткани или некий геометрический чертеж для плоской поверхности, в котором (как вы предполагаете) имеется элемент, повторяющийся непрерывно снова и снова, так что можно сделать эту поверхность настолько большой, насколько вам захочется. Это двумерный аналог задачи, которая решается в кристалле в трех измерениях.
Представьте, что вам нужно создать рисунок на обоях или ткани или некий геометрический чертеж для плоской поверхности, в котором (как вы предполагаете) имеется элемент, повторяющийся непрерывно снова и снова, так что можно сделать эту поверхность настолько большой, насколько вам захочется. Это двумерный аналог задачи, которая решается в кристалле в трех измерениях.
На рис. 30.1,а показан общий характер рисунка бумажных настенных обоев. Один элемент повторяется регулярно, и это может продолжаться бесконечно. Геометрические характеристики этого рисунка обоев, учитывающие только его свойства повторяемости и не касающиеся геометрии самого цветка или его художественных достоинств, показаны на рис. 30.1,6.
Если вы возьмете за отправную какую-то точку, то сможете найти соответствующую точку, сдвигаясь на расстояние а в направлении, указанном стрелкой 1. Вы можете попасть в соответствующую точку, также сдвинувшись на расстояние b в направлении, указанном другой стрелкой. Конечно, имеется еще много других направлений. Так, вы можете из точки а отправиться в точку c и достигнуть соответствующего положения, но такой шаг можно рассматривать как комбинацию шага в направлении 1 вслед за шагом в направлении 2.
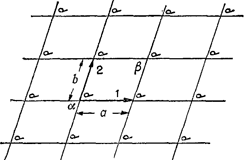 Одно из основных свойств ячейки состоит в том, что ее можно описывать двумя кратчайшими шагами к соседним эквивалентным расположениям. Под "эквивалентными" расположениями мы подразумеваем такие, что в каком бы из них вы ни находились, поглядев вокруг себя, вы увидите точно то же самое, что и в любом другом положении. Это фундаментальное свойство кристаллов. Единственное различие в том, что кристалл имеет трехмерное, а не двумерное расположение и, естественно, каждый элемент решетки представляет не цветы, а какие-то образования из атомов, например шести атомов водорода и двух атомов углерода, регулярно повторяющихся. Порядок расположения атомов в кристалле можно исследовать экспериментально с помощью дифракции рентгеновских лучей. Мы кратко упоминали об этом методе раньше и не будем добавлять здесь к сказанному чего-либо, а отметим лишь, что точное расположение атомов в пространстве установлено для большинства простых кристаллов, а также для многих довольно сложных кристаллов.
Одно из основных свойств ячейки состоит в том, что ее можно описывать двумя кратчайшими шагами к соседним эквивалентным расположениям. Под "эквивалентными" расположениями мы подразумеваем такие, что в каком бы из них вы ни находились, поглядев вокруг себя, вы увидите точно то же самое, что и в любом другом положении. Это фундаментальное свойство кристаллов. Единственное различие в том, что кристалл имеет трехмерное, а не двумерное расположение и, естественно, каждый элемент решетки представляет не цветы, а какие-то образования из атомов, например шести атомов водорода и двух атомов углерода, регулярно повторяющихся. Порядок расположения атомов в кристалле можно исследовать экспериментально с помощью дифракции рентгеновских лучей. Мы кратко упоминали об этом методе раньше и не будем добавлять здесь к сказанному чего-либо, а отметим лишь, что точное расположение атомов в пространстве установлено для большинства простых кристаллов, а также для многих довольно сложных кристаллов.
Внутреннее устройство кристалла проявляется по-разному. Во-первых, связующая сила атомов в определенных направлениях сильнее, чем в других направлениях. Это означает, что имеются определенные плоскости, по которым кристалл разбить легче, чем в других направлениях. Они называются плоскостями спайности. Если кристалл расколоть лезвием ножа, то скорее всего он расщепится именно вдоль такой плоскости. Во-вторых, внутренняя структура часто проявляется в форме кристалла.
Представьте себе, что кристалл образуется из раствора. В растворе плавают атомы, которые в конце концов пристраиваются, когда находят положение, отвечающее наименьшей энергии. (Все происходит так, как если бы обои были созданы из цветов, плавающих в разных направлениях до тех пор, пока случайно один из цветков не зацепился бы накрепко за определенную точку, за ним другой и т. д., пока постепенно не образовался узор.) Вы, вероятно, догадываетесь, что в одних направлениях кристалл будет расти быстрее, чем в других, создавая по мере роста некоторую геометрическую форму. Именно поэтому внешняя поверхность многих кристаллов носит на себе отпечаток внутреннего расположения атомов.
 В качестве примера на рис. 30.2,а показана типичная форма кристалла кварца, ячейка которого гексагональная (читайте материал о кварце с хорошими фото). Если вы внимательно посмотрите на этот кристалл, то обнаружите, что его внешние грани образуют не слишком хороший шестиугольник, потому что не все стороны имеют одинаковую длину, а часто бывают даже совсем разными. Но в одном отношении этот шестиугольник вполне правильный: углы между гранями составляют в точности 120o. Ясное дело, размер той или иной грани случайно складывается в процессе роста, но в углах проявляется геометрия внутреннего устройства. Поэтому все кристаллы кварца имеют разную форму, но в то же время углы между соответствующими гранями всегда одни и те же.
В качестве примера на рис. 30.2,а показана типичная форма кристалла кварца, ячейка которого гексагональная (читайте материал о кварце с хорошими фото). Если вы внимательно посмотрите на этот кристалл, то обнаружите, что его внешние грани образуют не слишком хороший шестиугольник, потому что не все стороны имеют одинаковую длину, а часто бывают даже совсем разными. Но в одном отношении этот шестиугольник вполне правильный: углы между гранями составляют в точности 120o. Ясное дело, размер той или иной грани случайно складывается в процессе роста, но в углах проявляется геометрия внутреннего устройства. Поэтому все кристаллы кварца имеют разную форму, но в то же время углы между соответствующими гранями всегда одни и те же.
Внутреннее геометрическое устройство кристалла хлористого натрия (поваренная соль, кубики) также легко понять из его внешней формы. На рис. 30.2, б показана типичная форма крупинки соли. Это опять не совершенный куб, но грани действительно перпендикулярны друг другу. Более сложный кристалл - это слюда, он имеет форму, изображенную на рис. 30.2, в. Этот кристалл в высшей степени анизотропен - он очень прочен в одном направлении (на рисунке - горизонтальном) и его трудно расколоть, а в другом направлении он легко расщепляется (в вертикальном). Обычно он используется для получения очень прочных, тонких листов. Слюда и кварц - примеры природных минералов, содержащих кремний. Третий минерал, содержащий кремний, - это асбест, обладающий тем интересным свойством, что его легко растянуть в двух направлениях, а в третьем он не поддается растягиванию. Создается впечатление, что он сделан из очень прочных нитей.
§ 2. Химические связи в кристаллах
Механические свойства кристаллов несомненно зависят от рода химических связей между атомами. Поражающая неодинаковая прочность слюды по разным направлениям зависит от характера межатомной связи в этих направлениях. Вам наверняка уже рассказывали на лекциях по химии о разных типах химических связей. Прежде всего бывают ионные связи, мы уже говорили о них, когда толковали о хлористом натрии. Грубо говоря, атомы натрия теряют по одному электрону и становятся положительными ионами; атомы хлора приобретают электрон и становятся отрицательными ионами. Положительные и отрицательные ионы располагаются в трехмерном шахматном порядке и удерживаются вместе электрическими силами.
 Ковалентная связь (когда электроны принадлежат одновременно двум атомам) встречается чаще и обычно более прочна. Так, в алмазе атомы углерода связаны ковалентными связями с ближайшими соседями в четырех направлениях, поэтому-то кристалл такой твердый. Ковалентная связь имеется и в кристалле кварца между кремнием и кислородом, но там связь на самом деле только частично ковалентная. Поскольку там электроны распределяются неравномерно между двумя атомами, атомы частично заряжены и кристалл до некоторой степени ионный. Природа не так проста, как мы пытаемся ее представить: существуют всевозможные градации между ковалентной и ионной связями.
Ковалентная связь (когда электроны принадлежат одновременно двум атомам) встречается чаще и обычно более прочна. Так, в алмазе атомы углерода связаны ковалентными связями с ближайшими соседями в четырех направлениях, поэтому-то кристалл такой твердый. Ковалентная связь имеется и в кристалле кварца между кремнием и кислородом, но там связь на самом деле только частично ковалентная. Поскольку там электроны распределяются неравномерно между двумя атомами, атомы частично заряжены и кристалл до некоторой степени ионный. Природа не так проста, как мы пытаемся ее представить: существуют всевозможные градации между ковалентной и ионной связями.
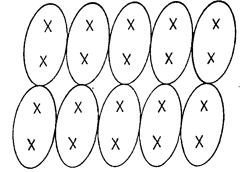
Кристалл сахара обладает другим типом связи. Он состоит из больших молекул, атомы которых сильно связаны ковалентной связью, так что молекула образует прочную структуру. Но так как сильные связи вполне насыщены, то между отдельными молекулами имеется относительно слабое притяжение. В таких молекулярных кристаллах молекулы сохраняют, так сказать, свою индивидуальность, и внутреннее устройство можно изобразить так, как на рис. 30.3. Поскольку молекулы не очень крепко держатся друг за друга, то кристалл легко можно расколоть. Такого рода кристаллы резко отличаются от кристаллов типа алмаза, который есть не что иное, как одна гигантская молекула, не поддающаяся разлому без того, чтобы не нарушить сильные ковалентные связи.
Другим примером молекулярного кристалла может служить парафин. Предельным случаем молекулярного кристалла являются вещества типа твердого аргона. Там притяжение между атомами незначительно - каждый атом представляет собой вполне насыщенную одноатомную "молекулу". Но при очень низких температурах тепловое движение настолько слабо, что крошечные межатомные силы могут заставить атомы расположиться в правильном порядке, подобно картофелинам, тесно набитым в кастрюле.
Металлы образуют совсем особый класс веществ. Там связь имеет совершенно другой характер. В металле связь возникает не между соседними атомами, а является свойством всего кристалла. Валентные электроны принадлежат не одному-двум атомам, а всему кристаллу в целом. Каждый атом вкладывает свой электрон в общий запас электронов, и положительные атомные ионы как бы плавают в океане отрицательных электронов. Электронный океан, подобно клею, удерживает ионы вместе.
Поскольку в металлах нет особых связей в каком-то определенном направлении, то там связь слабо зависит от направления. Однако металлы - это еще кристаллические тела, потому что полная энергия принимает наименьшее значение, когда ионы образуют упорядоченную систему, хотя энергия наиболее выгодного расположения обычно ненамного ниже других возможных расположений. В первом приближении атомы многих металлов подобны маленьким шарикам, упакованным с максимальной плотностью.
